プレスリリース
遺伝性ニューロパチーに対する新たな治療戦略を提案
MFN2関連Charcot-Marie-Tooth病モデルにおいて アルギニンが運動機能と生存率を改善
鹿児島大学病院 脳神経内科の安藤 匡宏講師、高嶋 博教授らの研究グループの研究成果が2026年4月3日(英国時間)に、国際学術雑誌「Neurotherapeutics」に掲載されましたことをお知らせいたします。
研究グループは、MFN2 遺伝子の異常によって生じる遺伝性末梢神経障害「シャルコーマリートゥース病(CMT2A)」に対し、アミノ酸の一種であるL-アルギニンが運動機能や生存率を改善する可能性を明らかにし、新たな治療法の候補となる可能性を示しました。
【趣旨等】
・MFN2遺伝子変異はシャルコーマリートゥース病(CMT2A)の主要な原因であるが、有効な薬物治療は確立されていません。
・本研究ではショウジョウバエモデルを用いてアルギニンの治療効果を検証しました。
・アルギニンが運動機能および生存率を改善することを明らかにし、新たな治療候補となる可能性を示しました。
【研究の背景】
遺伝性末梢神経障害(IPN)は、四肢遠位の筋力低下や感覚障害を呈する疾患群であり、その代表がシャルコーマリートゥース病(CMT)です。
MFN2遺伝子はミトコンドリア外膜に存在し、ミトコンドリア融合および細胞内エネルギー恒常性維持に重要な役割を担っています。この遺伝子の機能異常はミトコンドリアダイナミクスの破綻を引き起こし、神経変性の原因となりますが、現在有効な治療法は存在していません。
一方、L-アルギニンはミトコンドリア関連疾患であるミトコンドリア脳筋症(MELAS)において、病態機序に基づく治療として臨床応用されており、その有効性が報告されています。そこで本研究では、ミトコンドリア機能異常を背景とする遺伝性ニューロパチーに対する治療候補として、L-アルギニンに着目しました。
【研究の概要・成果】
本研究では、ショウジョウバエにおいてMFN2の相同遺伝子(Marf)を神経特異的に抑制したモデルを用い、アルギニン投与の効果を検討しました。発達段階の解析では恒常的なノックダウン系を用い、成虫における解析では温度感受性遺伝子発現制御システム(Gal4/UAS/Gal80ts系)により成虫期から遺伝子発現を誘導しました。
その結果、以下の知見が得られました。
■ 発達段階での改善
・高用量アルギニン(10 mg/mL)により蛹化率および羽化率が有意に改善しました。
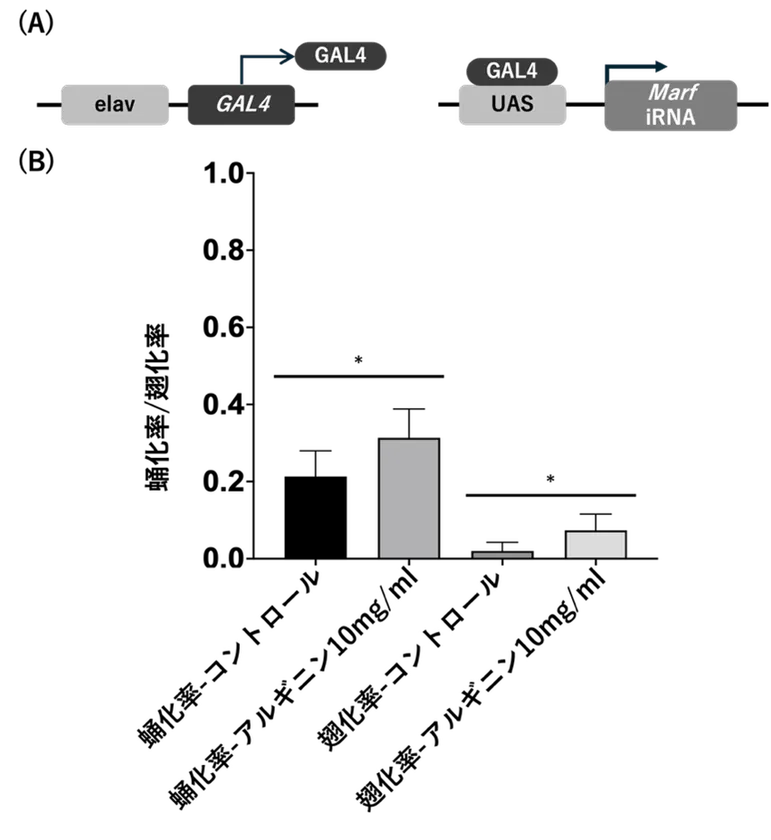
図1 MFN2ノックダウンショウジョウバエにおけるアルギニンの効果(A)実験系の模式図。神経特異的ドライバーであるelav-GAL4を用いて、UAS-Marf RNAiを発現させることで、ショウジョウバエにおいて神経特異的にMFN2相同遺伝子(Marf)をノックダウンした。(B)蛹化率および羽化率の比較。高用量アルギニン(10 mg/mL)投与により、蛹化率および羽化率はいずれもコントロールと比較して有意に改善した。
■ 運動機能の改善
・成体では時間経過とともに運動機能が低下しました。
・アルギニン投与により、day11およびday17で運動機能の改善を認めました。
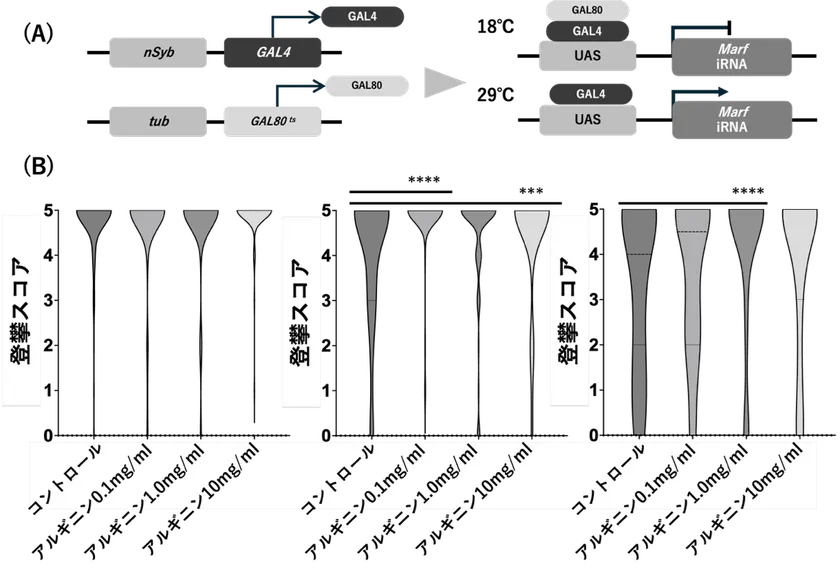
図2 MFN2ノックダウンショウジョウバエにおけるアルギニンの運動機能(A)実験系の模式図。nSyb-GAL4および温度感受性GAL80(GAL80ts)を用いた発現制御系により、成虫期において神経特異的にMFN2相同遺伝子(Marf)をノックダウンした。18℃ではGAL80によりGAL4活性が抑制されるが、29℃へ温度シフトすることでGAL80の抑制が解除され、Marf RNAiの発現が誘導される。 (B)登攀スコアの経時的変化。day3、day11、day17において運動機能(登攀能力)を評価した。day3では有意差を認めなかったが、day11では0.1 mg/mLおよび10 mg/mLのアルギニン投与群で有意な改善を認めた。day17では1 mg/mL群で最も顕著な改善を認めた。データは分布(バイオリンプロット)として示す。*p<0.05、***p<0.001、****p<0.0001。
■ 生存率の改善
・高用量アルギニンにより生存期間の延長を認め、特に早期死亡の抑制効果が示唆されました。
■ ミトコンドリアストレス下での効果
・ロテノン(ミトコンドリア複合体I阻害剤)により生存率は低下しました。
・高用量アルギニンにより生存率は有意に改善しました。
【今後の展望】
本研究は、CMTの治療法開発においてミトコンドリア機能に着目し、MFN2関連遺伝性ニューロパチーに対する新たな治療候補としてアルギニンの有用性を示したものです。
ミトコンドリア機能異常に対する代謝的アプローチにより、神経細胞の生存を改善し得る可能性が示唆されました。
今後は、作用機序の解明を進めるとともに、変異導入ショウジョウバエモデルや他のモデル動物を用いた検証を行い、臨床応用に向けた研究を発展させていく予定です。
【研究成果の公表】
これらの研究成果は、2026年4月3日に国際学術雑誌「Neurotherapeutics」に掲載されました。
<タイトル>
Arginine ameliorates motor and survival deficits in MFN2-Deficient Drosophila models
<著者名>
Masahiro Ando, Yuji Okamoto, Yujiro Higuchi, Jun-Hui Yuan, Akiko Yoshimura, Chikashi Yano, Risa Nagatomo, Takahiro Hobara, Fumikazu Kojima, Yu Hiramatsu, Satoshi Nozuma,
Yusuke Sakiyama, Hiroshi Takashima
<DOI>
https://doi.org/10.1016/j.neurot.2026.e00900
本研究は、厚生労働科学研究費補助金(2016100002B)、日本医療研究開発機構(AMED)(201442014A、201442071A)、ならびに日本学術振興会科学研究費助成事業(JP18H02742、JP20K16604、JP21K15702、JP21H02842、JP22K15713、JP22K07495、JP22K07519、JP23K06931、JP23K06966)の支援を受けて実施されました。
本研究の遂行にあたり、ご協力いただきました関係者の皆様に深く感謝申し上げます。
【補足説明】
※1 遺伝性末梢神経障害(IPN)
遺伝的原因により末梢神経の障害が引き起こされる疾患群であり、その代表がCharcot-Marie-Tooth病である。四肢遠位筋の進行性筋力低下や筋萎縮、感覚障害を特徴とする。CMTの有病率は約2500人に1人とされている。
※2 MFN2遺伝子
ミトコンドリア外膜に存在するタンパク質mitofusin-2をコードし、ミトコンドリア融合や細胞内エネルギー代謝の維持に重要な役割を担う。変異はCharcot-Marie-Tooth病2A型の原因となる。日本においては、CMTの原因遺伝子として3番目に多いことが報告されている。
※3 ミトコンドリアダイナミクス
ミトコンドリアの融合と分裂のバランスによって維持される動的な構造変化のことであり、細胞のエネルギー産生や品質管理に重要である。
※4 L-アルギニン
アミノ酸の一種であり、一酸化窒素(NO)の前駆体として血流改善やミトコンドリア機能に関与することが知られている。ミトコンドリア脳筋症(MELAS)に対する治療として臨床的に使用されている。
【鹿児島大学について】
鹿児島大学は、9つの学部と9つの大学院研究科を擁する、南九州における最高学府です。南九州から南西諸島など南北600キロに及ぶ県土を本学のキャンパスとして、そこにある自然・歴史・風土・産業を土台に活動しています。地域とともにある大学として「知」と「智」の力をもって、“進取の精神で、地域と世界の未来に挑む教育研究拠点”となることを目指して進んで参ります。
鹿児島大学HP : https://www.kagoshima-u.ac.jp/
鹿児島大学Instagram: https://www.instagram.com/kagoshima_univ.koho/
鹿児島大学病院HP : https://www.hosp.kagoshima-u.ac.jp/