報道関係者各位
プレスリリース
2019.12.03 10:30
日本メナード化粧品株式会社
日本メナード化粧品、肌のターンオーバーにおける新発見!
~ダメージを受けた細胞が、優先的に排出される~
日本メナード化粧品株式会社(名古屋市中区丸の内3-18-15、代表取締役社長:野々川 純一)は、藤田医科大学(豊明市沓掛町田楽ヶ窪1-98)の応用細胞再生医学講座(教授:赤松 浩彦)および皮膚科学講座(教授:杉浦 一充)との共同研究によって、肌のターンオーバーにおいて紫外線ダメージを受けた細胞が優先的に排出されていることを発見しました。また、加齢に伴いこの細胞の排出が低下することでダメージを受けた細胞が蓄積されてしまうことを見出しましたので報告いたします。
今回の発見から、これからの美容の新しいターゲットとして、ダメージを受けた細胞の排出を促進させることが重要であると考えられました。
肌の表皮は、約28日間かけて生まれ変わっていることが知られています。また、この肌の生まれ変わりは加齢により遅延し、それに伴い肌の機能が低下することが明らかになっています。この肌の生まれ変わりは「ターンオーバー」と呼ばれ、これまでも美容において重要な生理現象として研究が進められていますが、未だ不明な点が多く残されています。
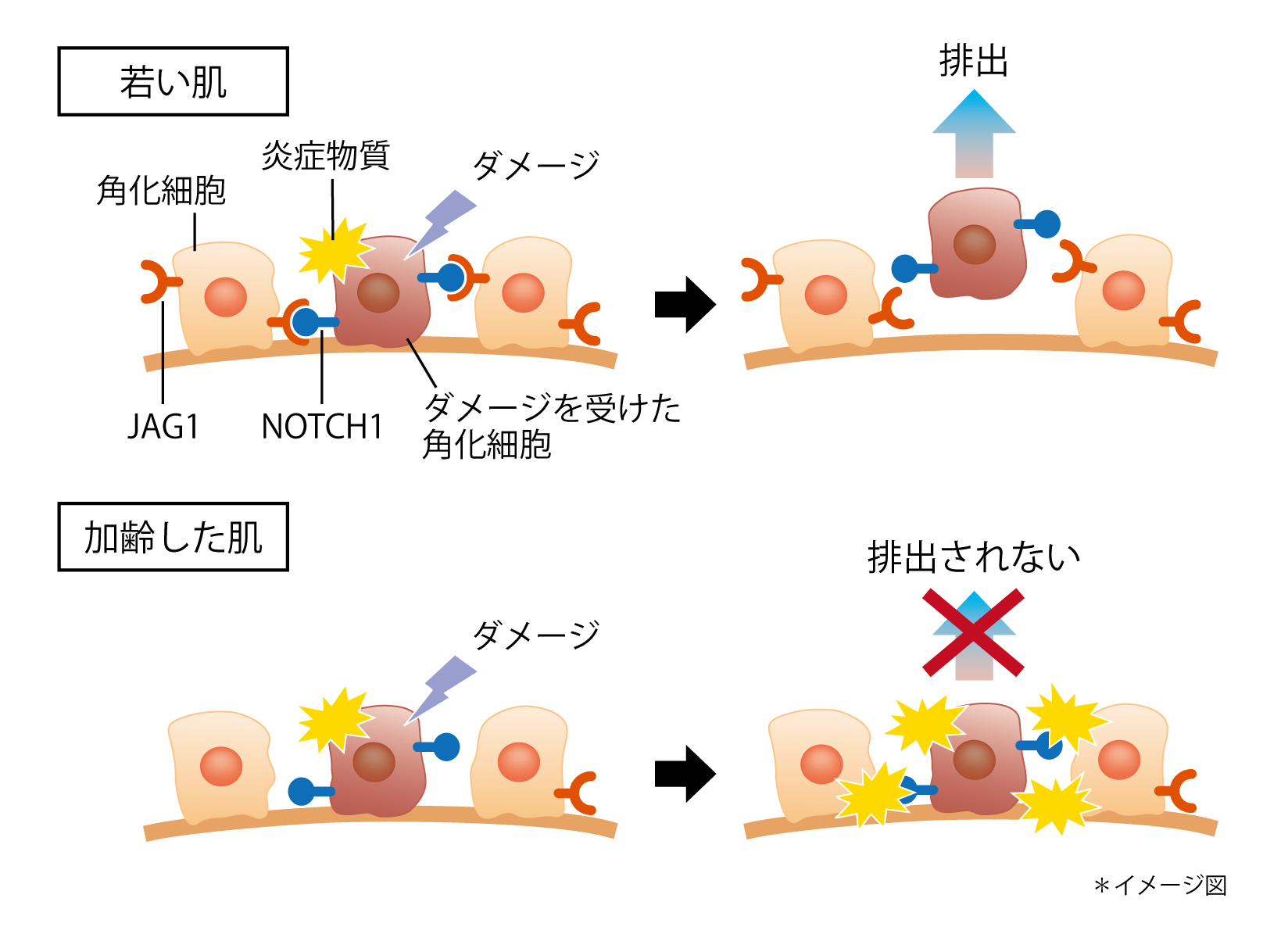
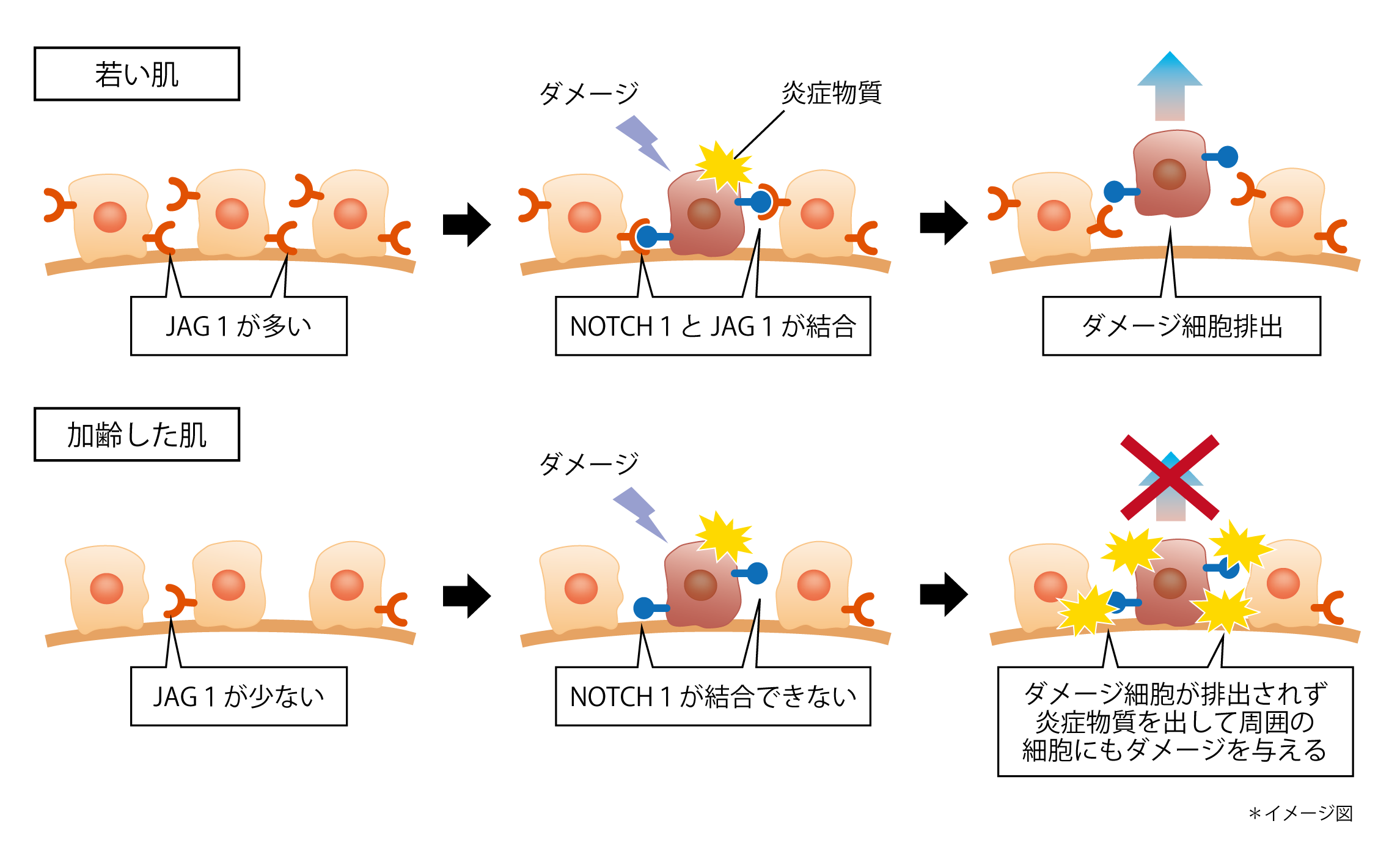
今回、肌の表皮を構成する角化細胞に紫外線を照射した結果、紫外線でダメージを受けた細胞(ダメージ細胞)では「NOTCH1」と呼ばれるタンパク質の発現が特異的に高まることを突き止めました。また、NOTCH1が周囲の角化細胞の「JAG1」と呼ばれるタンパク質に結合すると、NOTCH1を発現する細胞が優先的に排出されることが分かりました。つまり、肌のターンオーバーにおいて、ダメージ細胞が優先的に排出されていることが分かりました。また、加齢によって角化細胞のJAG1の発現が減少することから、JAG1とNOTCH1が結合する機会が減少することでダメージ細胞が蓄積し、肌の老化が進行すると考えられました。
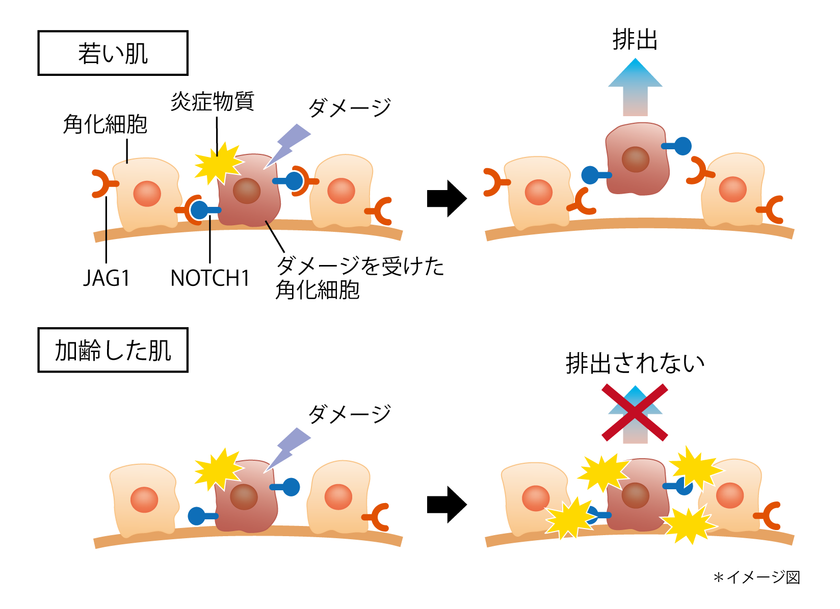
ダメージ細胞排出メカニズム
近年、ダメージ細胞の蓄積が身体の老化原因のひとつと考えられています。今回このメカニズムを発見したことで、メナードでは新しい美容のターゲットとして“ダメージ細胞の排出を促進させる”というアプローチについてさらに研究を進めます。なお、本研究の成果は2019年12月3日から6日にかけて福岡国際会議場、マリンメッセ福岡で開催される第42回日本分子生物学会年会にて発表します。
<参考資料>
1. ダメージを受けた細胞について
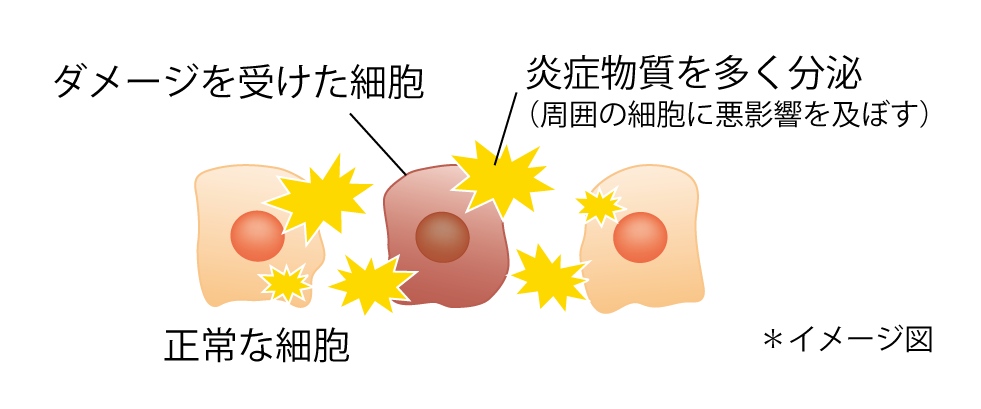
私たちの身体に存在する多くの細胞は紫外線や活性酸素によってダメージを受けます。ダメージが蓄積した細胞は機能が低下するとともに、炎症性サイトカインなどを分泌して炎症を引き起こし、組織に損傷を与えます。また近年では、身体の様々な組織において、加齢とともにダメージを受けて機能が低下した細胞が蓄積することが発見されています。したがって、ダメージを受けた細胞が蓄積することにより、組織の老化が加速すると考えられます。
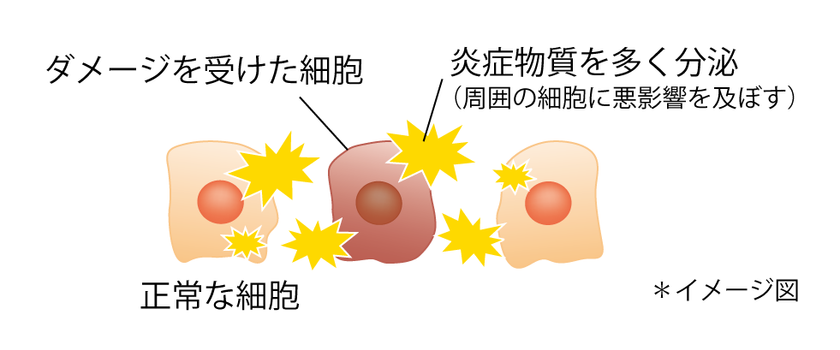
図1 ダメージ細胞は周囲の細胞へ悪影響を及ぼす
2. 肌においてダメージ細胞が優先的に排出されるメカニズム
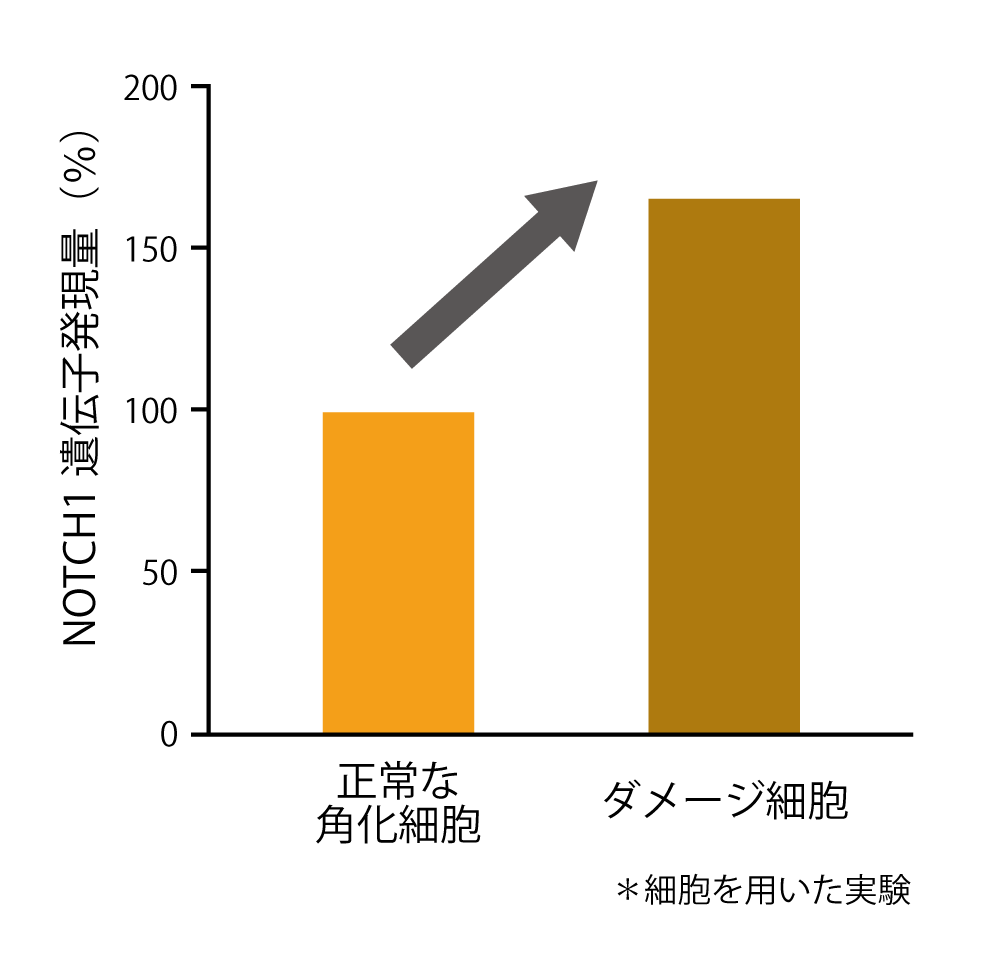
紫外線をくり返し照射しダメージを与えた角化細胞(ダメージ細胞)の遺伝子発現を解析した結果、ダメージ細胞では「NOTCH1」と呼ばれるタンパク質の発現が高いことが分かりました(図2)。NOTCH1は細胞の表面に発現するタンパク質で、隣接する細胞の表面に発現するタンパク質「JAG1」と結合します。
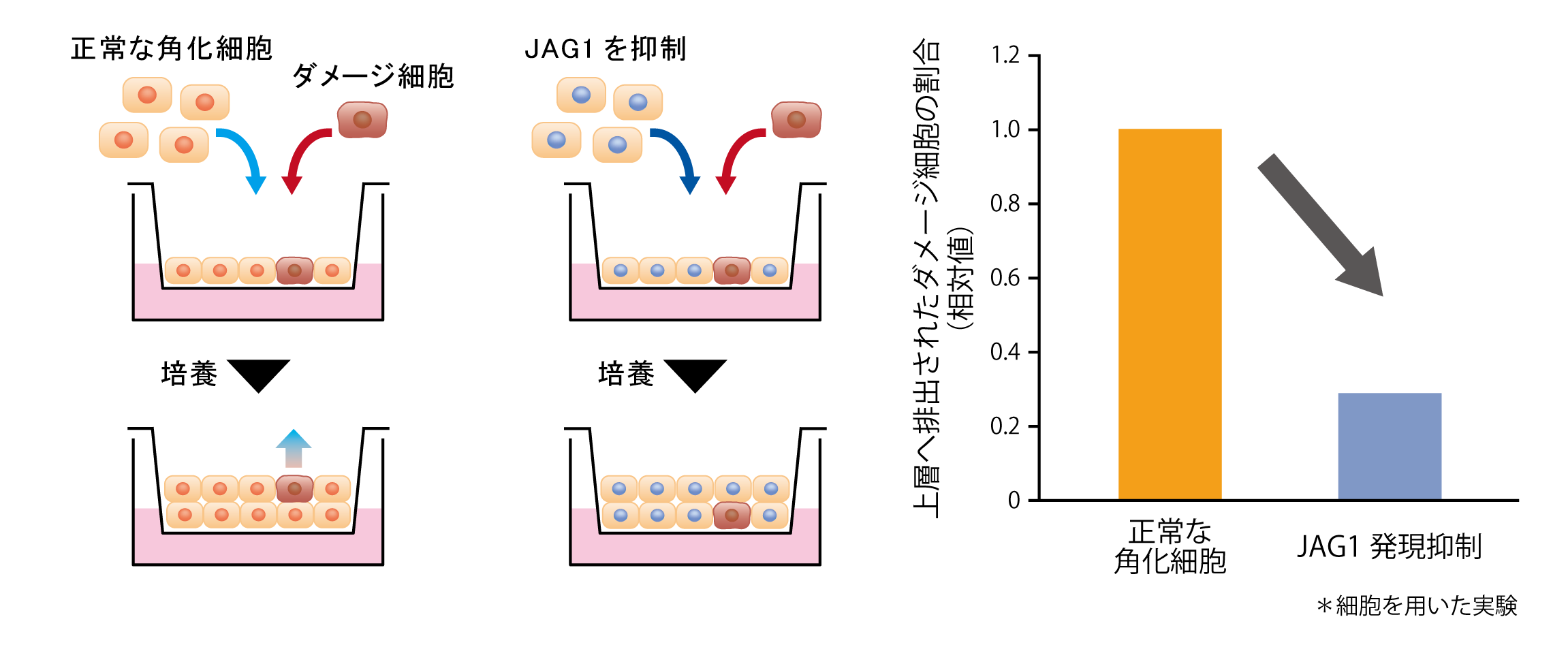
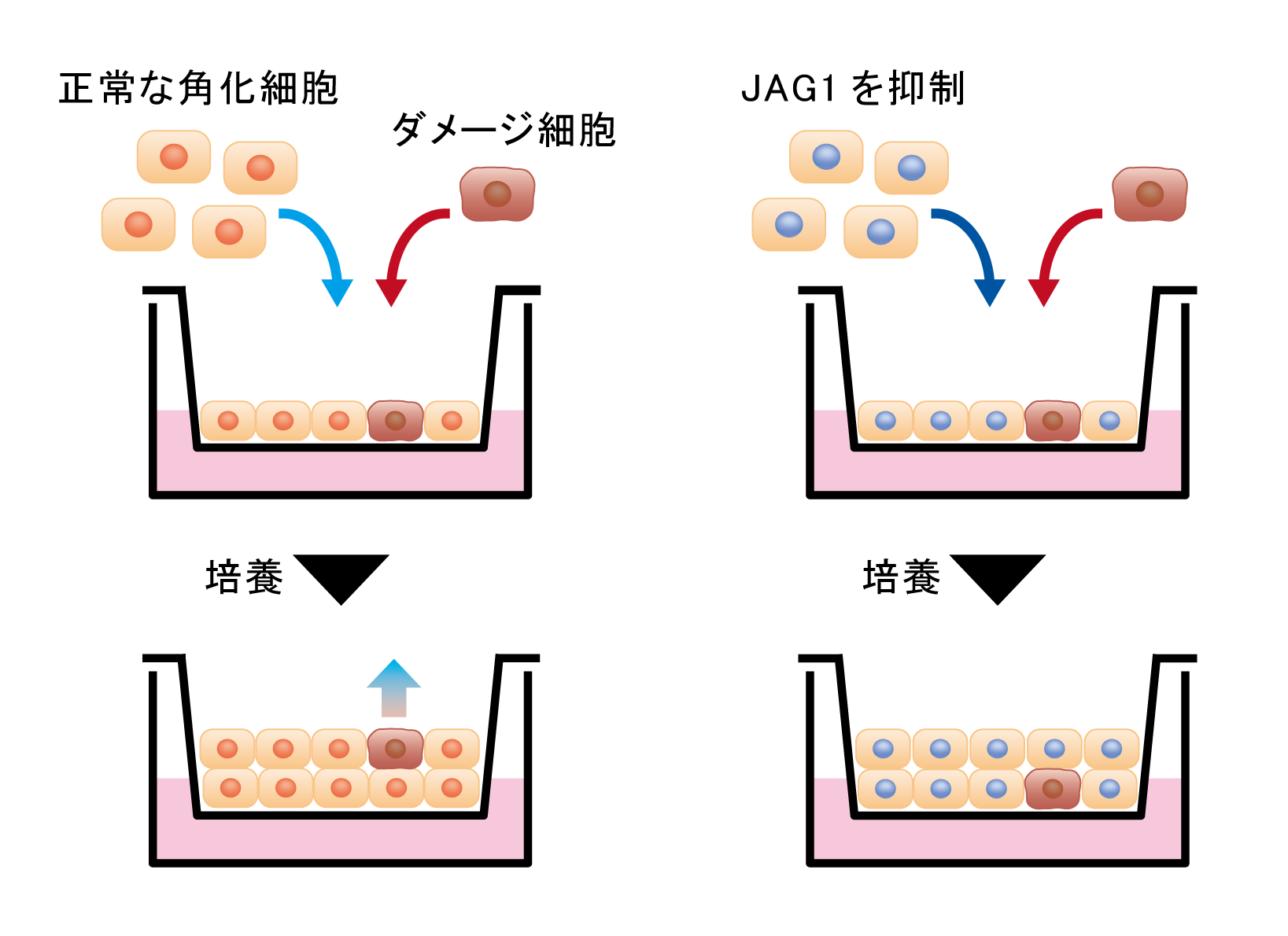
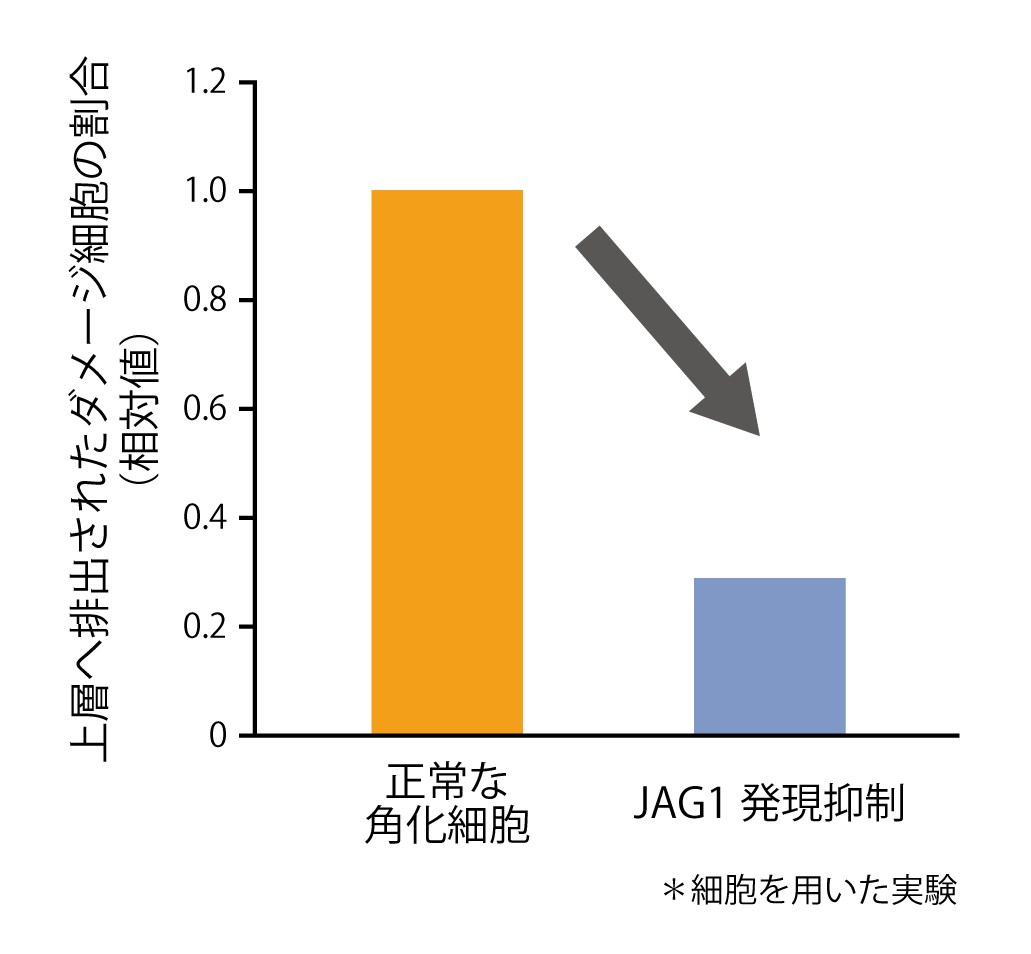
また、正常な角化細胞(JAG1を発現)とダメージ細胞(NOTCH1を発現)を混合し培養したところ、ダメージ細胞が優先的に排出されることが明らかになりました。この時、正常な角化細胞のJAG1の発現を抑制すると、ダメージ細胞が排出されにくくなりました(図3)。このことから、ダメージ細胞の排出には正常な角化細胞のJAG1の発現が重要であることが分かりました。
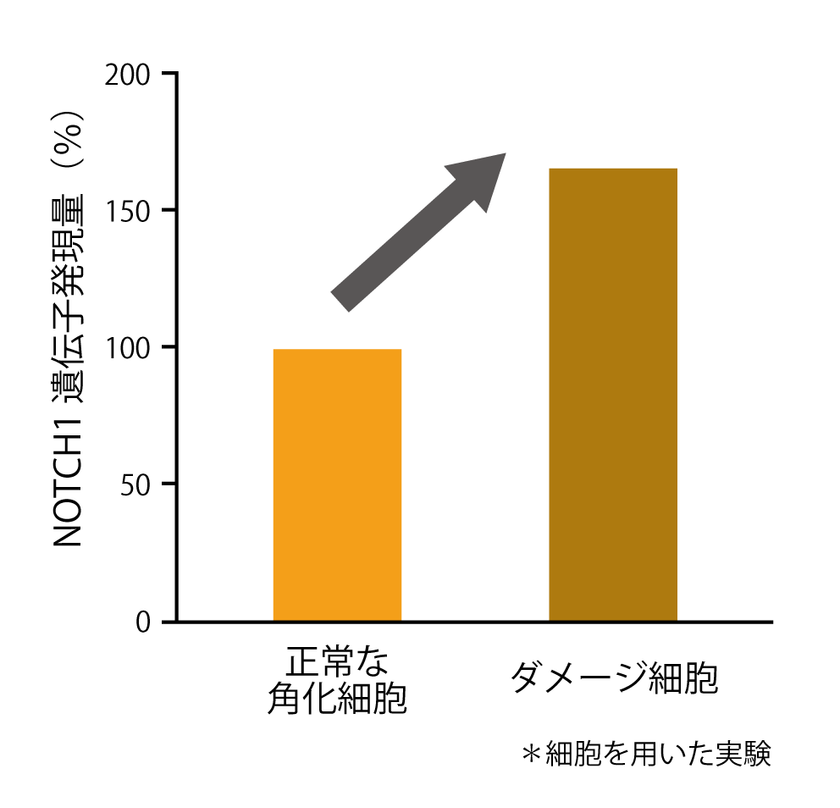
図2 ダメージ細胞のNOTCH1遺伝子発現
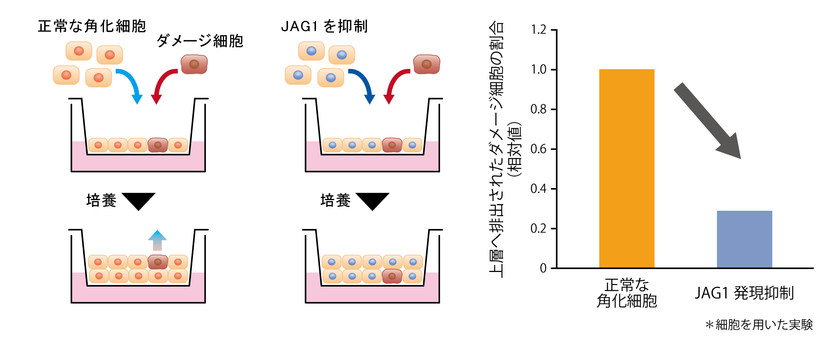
図3 ダメージ細胞排出におけるJAG1の影響
3. 加齢によりダメージ細胞が蓄積する
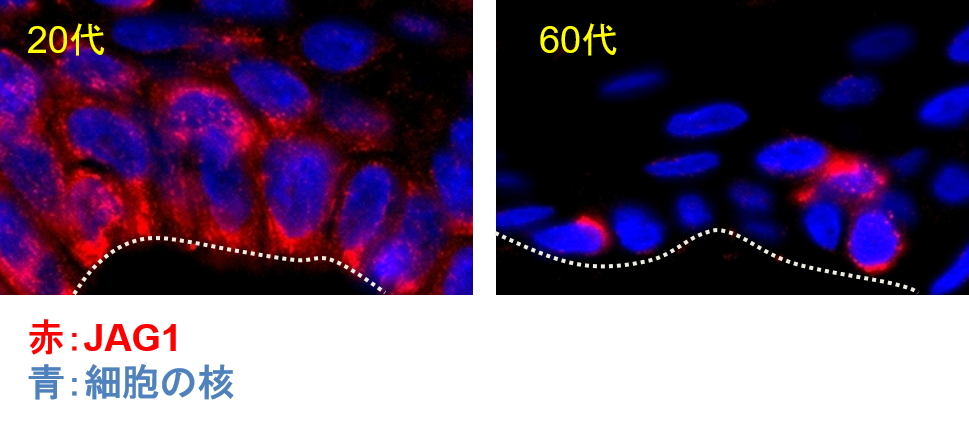
ヒトの表皮におけるJAG1の発現を確認したところ、加齢によって角化細胞のJAG1の発現が低下していることが分かりました(図4)。このことから、加齢した肌ではダメージ細胞のNOTCH1に結合するためのJAG1が減少しているため、ダメージ細胞が排出されずに蓄積すると考えられました(図5)。
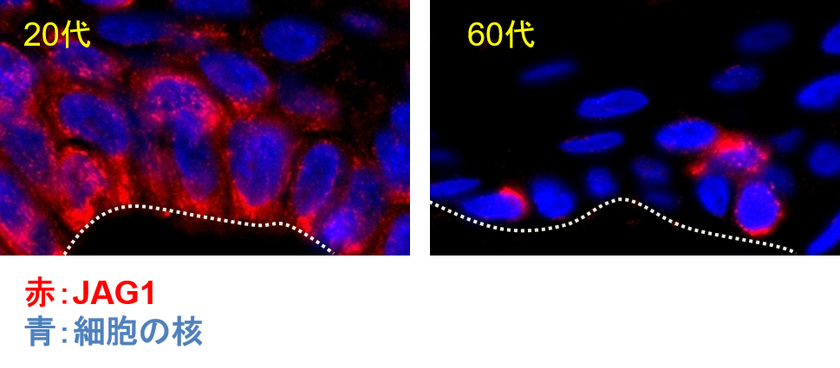
図4 ヒト表皮におけるJAG1発現の加齢変化
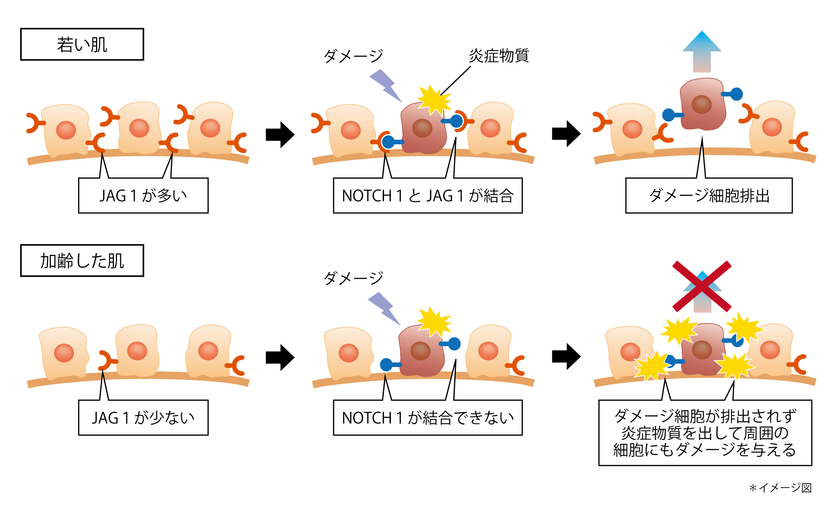
図5 加齢によりダメージ細胞が排出されなくなるメカニズム